細胞培養
細胞培養への工学的なアプローチが求められる時代になっております。細胞の成長の環境を整えることや、細胞の動きを動的に観察し細胞からの情報を得ること、細胞融合の際の環境、細胞増殖の際の環境などに現代科学の手法が適用されることが求められています。
弊社のこれまでの細胞に関する経験を紹介し、これからの細胞培養等の技術展開の参考にしていただければ幸いです。キャピラリー電気泳動による赤血球のシングルセルレベルでの分離
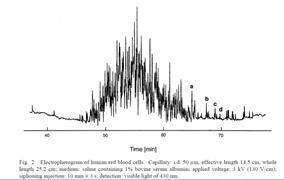
ヒトの赤血球は、脊髄で作られ時間がたつと死滅していきます。すなわち血液中の赤血球は、若い血球と古い血球が混在しています。これらは赤血球膜表面の電荷の状態にも反映します。装置はキャピラリーカラム(内径50マイクロメートル、有効長20mm)中に赤血球を注入し、電場下での赤血球の移動を見ますと分布のあるパターンになります(図1参照)。すなわち電気移動度の異なった個々の血球に分散していることが分かります。本方法により、血球の個々の移動度と全体の分散が求められます(文献[1])。
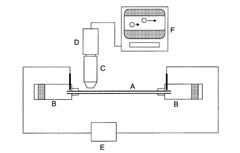
A: キャピラリー管、C: マイクロスコープ
赤血球キャピラリーカラムの作成
赤血球を充填剤として詰めたキャピラリーカラムを作成し、このカラムを用いてピリドキサミンやセロトニンが赤血球の膜を経由して赤血球内部にいたり別の化合物に変化するのを見出しました。赤血球のカラム(図2参照)は赤い色をして、作成後電場下では約一時間は安定しており、この間に実験を実施しました。電場を印加しない時は2~3日安定でした。赤血球カラムの試みは、細胞の群としての挙動を検討する一つの手段として成り立ちます(文献[2])。
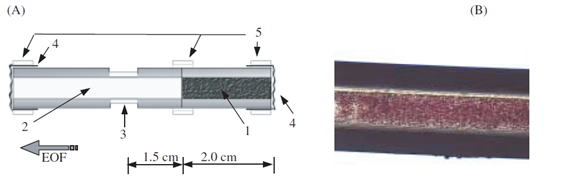
1: 赤血球カラム、4: アガロースゲル(キャップ)
糖尿病疾患の血液細胞の電気泳動分布と疾病の重症度との関連
赤血球の個々の細胞の電気泳動を調べその分布と重症度との関連を調べました。疾病の及ぼす影響が個々の赤血球の電気移動度に反映され、また移動速度分布に反映されていることが分かりました。小型のキャピラリーカラムを用い、細胞を光学的に測定してカウントします(文献[3])。
赤血球の細胞膜の溶解
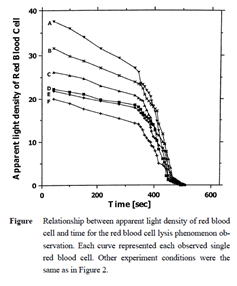
赤血球の一細胞の膜の溶解を、顕微鏡下で溶解液の流れの中で観察しました。溶解液として0.03%の過酸化水素を含む生理食塩水を電気浸透流で細胞に導き、細胞膜の溶解のプロセスを1000倍の顕微鏡で一個のセルごとに観察しました。溶解には約400秒の時間を要しました。膜が損傷し形態が変化し、次いで細胞内液が流出するのが観察できました(文献[4])。
赤血球の電気移動度
無重力下での赤血球の電気移動度は、1G(地上)での電気移動度より約30%高い値を示しました。これは細胞の無重力下でのフローティングによる影響と思われます。装置は非常に小型のセル泳動装置を作成し、1000倍の画像で細胞の挙動を捉えました。実験は飛行機のパラボリックフライトによる無重力時の環境下で測定しています(文献[5])。
血液判定
細胞の表面の電荷を利用して、血液判定を試みました。すなわち赤血球は表面電荷がプラスで、血漿はマイナスまたは中性の電荷を有しますので、両者はキャピラリー管中で互いに出会うことができます。この血漿が赤血球と異なるタイプである時血球の凝集が観察できます。血液型判定が微小空間で可能となります。装置は10mmのキャピラリー管(内径50マイクロメートル)とCCDカメラで構成しました(文献[6])。
単一細胞のマニピュレィション
神経芽細胞一個をガラス製のキャピラリー管内部に取り込む方法として、培養液がキャピリー管内部に入り込まない方法を提案しました。キャピラリー内部から常に新鮮な液を電気浸透流により培地に注ぎながら、その流れに抗して細胞をキャピラリー内部へ洗浄しながら細胞を取り込むことが出来ます。この原理は細胞表面が正電荷を持っていること、キャピラリー管内部が負の電荷を持っていることの利用で実現できます(文献[7])。
極微量インジェクターの製作
一細胞の内溶液や極微小領域の溶液を採集して、局所の情報を得ることが細胞を取り扱うには重要な事柄です。今まで液体クロマトグラフィーにおける注入方法はサブマイクロリットルが限界でした。ローター内部の試料を採集する小さな穴の製作に限界がありました。この穴にキャピラリー管を埋めこむことにより20ナノリットルのインジェクターが開発できました。タンパクの測定などマイクロからナノ液体クロマトグラフィー領域における唯一のインジェクターを作成できました(文献[8])。
顕微鏡ステージ上へのクロマトグラフシステム構築
極微量の資料の取り扱いには、非常に小さなクロマトグラフシステムが必須となります。特に一細胞の取り扱いを目指して、顕微鏡のステージ上にクロマトグラフシステムを構築しました(文献[9])。
これからの工学的アプローチ: 弊社の技術的な視点
培養細胞のセル内での増殖を図るには、セル内の環境の維持、クリーン化、自動的な保障システムの構築など様々な生命維持の観点からの工夫が必要になります。
システムには、微小なセンサーが必要とされます。
また新しい工夫や視点を変えた工夫などが必要です。小型の電導度システム、溶液の流れを感知するシステム、pH測定システム、培地の健康状態を検知するシステム、培地自体の検知系や間接的に培地からの発生ガスの検知システムが必要になるでしょう。これらの技術はミクロ化を追求してきました弊社の経験がお役に立てると考えております。
また香り、匂い、臭いが生命体の健康状態を反映しますので、培地の匂い検知システムに長年にわたってヒトの匂い、香りを検討してきた弊社の技術が貢献できると考えております。
文献
- Analytical Sciences, 16, 847-850, 2000.
- Analytical Sciences, 21, 453-456, 2005.
- ELECTROPHORESIS, 20: 2560–2565, 1999.
- Chromatography, 23, 33-38, 2002.
- Electrophoresis, 13, 2035-2039, 2002.
- 分析化学, 47, 355-359, 1998.
- Electrophoresis, 16, 1364-1368, 1995.
- Analytical Chemistry, 75, 3929-33, 2003.
- Chapter 9, Electrokinetic Phenomena: Principles and Applications in Analytical Chemistry and Microchip Technology, Marcel Dekker, 2004.